En química y física, átomo es la unidad más pequeña de un elemento químico que mantiene sus propiedades y que no es posible dividir mediante procesos químicos.
Un átomo esta constituido por 3 partes básicas como el electrón que tiene carga negativa, el protón que tiene carga positiva y el neutrón que no tiene carga.
El concepto de átomo nació en la antigua Grecia con ayuda de los filósofos DEMOCRITO, LEUCIPO Y EPICURO por que querían dar una explicación a la conformación de la materia.
Más tarde aparece un avance más, que es el postulado de “la materia no se crea ni se destruye, simplemente se transforma; este concepto fue dado por el químico ANTOINE LAURENT DE LAVOISIER. Al pasar el tiempo ocurre una evolución de descubrimientos con respecto al átomo; es ahí donde aparecen los modelos atómicos:
· El primero es de john Dalton: Que decía que la materia esta conformada por partículas muy pequeñas (átomos), los átomos de un elemento son iguales pero de otros son diferentes. Los compuestos aprecian de átomos de diferentes elementos.
· El segundo es el modelo de Thomson:

Donde se explica que el átomo tiene una parte negativa (electrones) y una parte positiva (protones); los electrones están en una carga positiva como si fueran pasas en una torta.
El tercero es el átomo de Rutherford:

El átomo se compone de una parte positiva y una negativa, sin embargo, a diferencia del anterior, postula que la parte positiva se concentra en un núcleo, el cual también contiene virtualmente toda la masa del átomo, mientras que los electrones se ubican en una corteza orbitando al núcleo en órbitas circulares
· El cuarto es el átomo de Bohr:

El átomo es un pequeño sistema solar con un núcleo en el centro y electrones moviéndose alrededor del núcleo en orbitas bien definidas.” Las orbitas están cuantizadas (los e- pueden estar solo en ciertas orbitas). Es estrictamente un modelo del átomo de hidrógeno
Cada orbita tiene una energía. La más externa es la de mayor energía. Los electrones pueden saltar de una a otra orbita.
· Y El quinto es el modelo actual o de Schrödinger:

Se abandona la concepción de los electrones como esferas diminutas con carga que giran en torno al núcleo. Describe a los electrones por medio de una función de onda, el cuadrado de la cual representa la probabilidad de presencia en una región delimitada del espacio. Esta zona de probabilidad se conoce como orbital.
MATERIA:
Denominamos materia a todo aquello que podemos percibir con nuestros sentidos, es decir, todo lo que podemos ver, oler, tocar, oír o saborear es materia. Toda la materia está formada por átomos y moléculas.
Un cuerpo es una porción de materia, delimitada por unas fronteras definidas, como un folio, el lápiz o la goma de borrar; varios cuerpos constituyen un sistema material.Las distintas formas de materia que constituyen los cuerpos reciben el nombre de sustancia. El agua, el vidrio, la madera, la pintura... son distintos tipos de sustancias.
La materia está en constante cambio. Las transformaciones que pueden producirse son de dos tipos:- Físicas: son aquellas en las que se mantienen las propiedades originales de la sustancia ya que sus moléculas no se modifican.- Químicas: son aquellas en las que las sustancias se transforman en otras, debido a que los átomos que componen las moléculas se separan formando nuevas moléculas.
Una propiedad física es una característica que puede ser estudiada usando los sentidos o algún instrumento específico de medida. Estas se manifiestan básicamente en los procesos físicos como cambios de estado, cambios de temperatura, cambios de presión, etc. Por ejemplo, color, dureza, densidad, punto de ebullición, punto de fusión.
Las propiedades químicas son propiedades distintivas de las sustancias que se observan cuando se combinan con otras, es decir, que les pasa en procesos por los que, por otra parte, las sustancias originales dejan generalmente de existir, formándose con la misma materia otras nuevas. Las propiedades químicas se manifiestan en las reacciones químicas.Algunas propiedades químicas de la materia son: reactividad, poder calorífico, acidez, etc.
Materia orgánica
Materia orgánica es estudiada por la química orgánica. Las moléculas orgánicas que constituyen la materia son derivadas del carbono.Metal tiene unoEl carbono puede combinarse consigo mismo infinidad de veces, y dar lugar a moléculas muy grandes y complejas.
Materia inorgánica
Estudiada por la química inorgánica. Está formada por moléculas más simples. La materia inorgánica no es derivada del carbono.
Materia viva
La materia viva es la materia que forma parte de los seres vivos. Puede ser orgánica (proteínas, lípidos, azúcares, etc.) y también puede ser inorgánica (agua, sales minerales).
LEY DEL OCTETO:
La ley del octeto dice que un átomo debe tener 8 electrones en su última capa para ser estable. Los gases nobles cumplen con esto y por esto son los más estables. Si no tienen los 8 electrones serán más reactivos y predispuestos a combinarse o reaccionar con otros átomos para alcanzar los 8 electrones y la estabilidad.Esto es la base de las reacciones químicas y la reactividad de átomos.
En síntesis, para completar el octeto el átomo debe tener completos sus niveles de energía. Hay elementos cuyos átomos ya tienen completo su octeto por naturaleza, como es el grupo de los gases nobles (8A... la ultima columna a la derecha de la tabla periódica).El número de valencia ó número de oxidación es el número de electrones de valencia que tiene completados el átomo. Por ejemplo, si trabaja con el número -2 es que tiene 2 electrones libres en su último nivel.
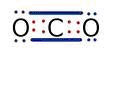

ESTE ENLACE NOS MUESTRA LA ACTIVIDAD ANTERIOR CON FORMATOS DEL SENA
http://www.scribd.com/doc/3262741/TAREA-1-TBT
http://www.scribd.com/doc/3262741/TAREA-1-TBT
No hay comentarios:
Publicar un comentario